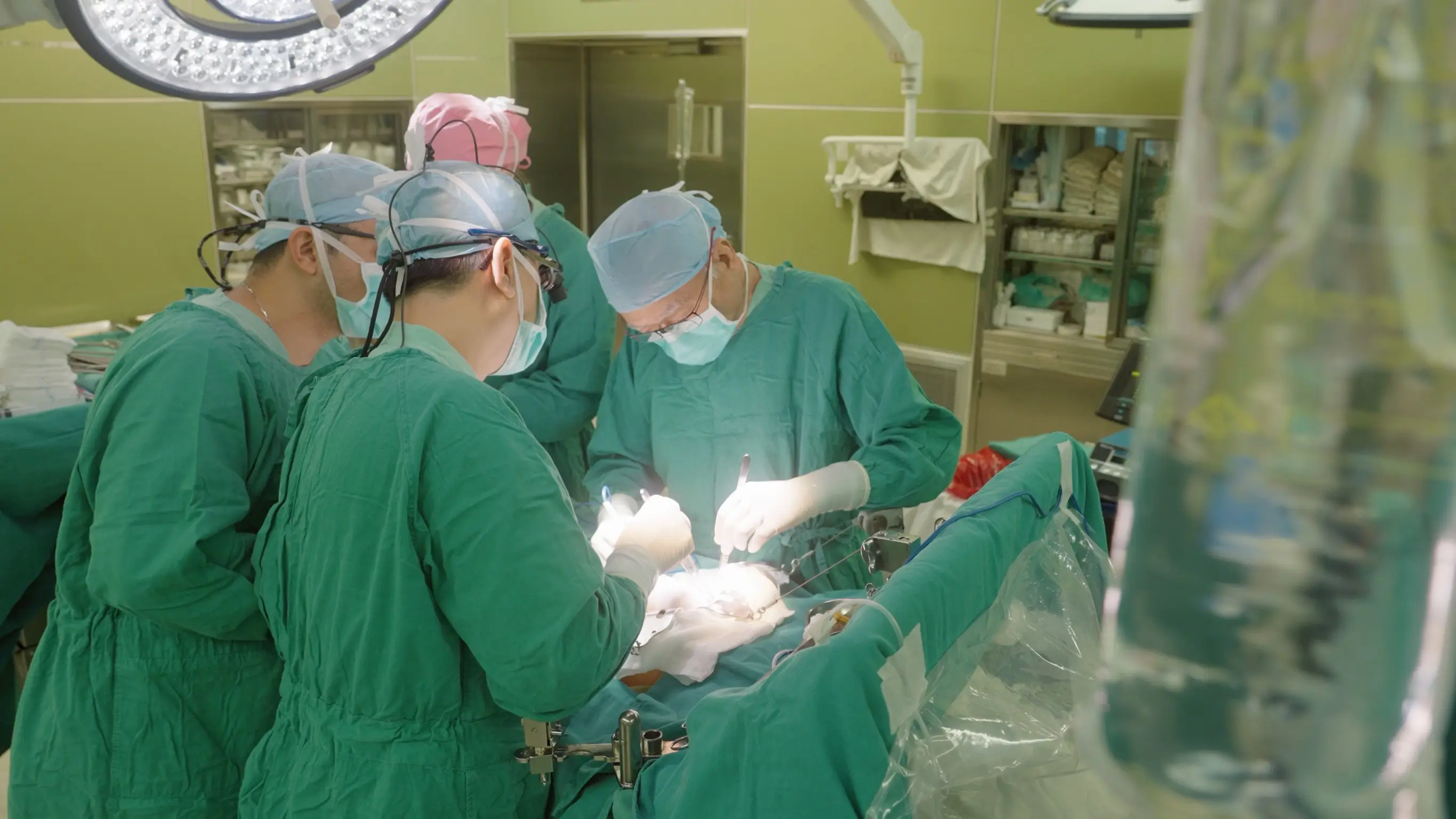
台灣臨床試驗量下滑!石崇良示警調整競爭策略 三方向優化


【記者林芳如/台北報導】臨床試驗已成為各國推動醫療創新與生醫產業發展的重要關鍵基礎建設,然而台灣第一期臨床試驗數量下降,衛福部長石崇良示警須調整競爭策略,前端朝三方向優化,包括簡化申請流程、推動聯合人體試驗委員會審查和文件一致性以加速核准時效、加快收案速度,後端搭配食藥署查驗登記加速、健保核價加成,確保國人能以更快速度用到新藥。
中華民國開發性製藥研究協會理事長胡耀中表示,台灣臨床試驗具備高品質與高潛力的發展基礎,根據調查,台灣有超過六成的機會成為全球前25%優先開立試驗點的國家,然而,目前臨床試驗啟動速度仍受限於多重行政程序,未來應參考澳洲、南韓、新加坡等國做法,才能在高度競爭的國際趨勢下脫穎而出。
衛福部長石崇良今日(3/26)出席「2026臨床試驗生態系白皮書發布」記者會,指出台灣這幾年臨床試驗總數,尤其是第一期臨床試驗數量逐年下降,這是重要警訊,影響整個國家用藥可近性,意味台灣必須調整競爭策略。
石崇良表示,當臨床試驗在台灣執行或曾經在台灣收案,未來申請藥證,更能確保種族差異性,能更精準地確認藥物對台灣人的療效與安全性,同時讓現有醫療手段無法治療的重症病患,有機會透過臨床試驗獲得最新治療,所以臨床試驗若能在台灣實施,不僅對病人好,對未來國外藥廠取得藥證進入台灣市場,也是一個非常重要的參考。


「台灣臨床試驗中心聯盟」去年成立,集結31家醫院,石崇良說,今年衛福部投入預算補助,協力朝三方向優化,第一,建立單一窗口,藥廠不需再逐一向各家醫院遞送計畫,簡化申請流程,第二,推動聯合 IRB(人體試驗委員會)審查,避免重複審理,推動文件一致性,包括合約、知情同意書等格式標準化,縮短行政往返時間。
第三,加快收案速度,透過聯盟機制讓多個中心同時啟動,縮短尋找病患與收案所需的總時程。除了上述前端部分,石崇良強調,後端搭配食藥署查驗登記加速,在台灣執行臨床試驗的藥品,縮短取得藥證的時間,以及針對在台灣執行臨床試驗的新藥,健保給付時給予藥價加成或更優渥的核價條件,鼓勵藥廠將新藥引進台灣。
石崇良表示,希望透過一系列做法的改革,確保台灣民眾能以更快的速度、用到更好且更新的藥物。