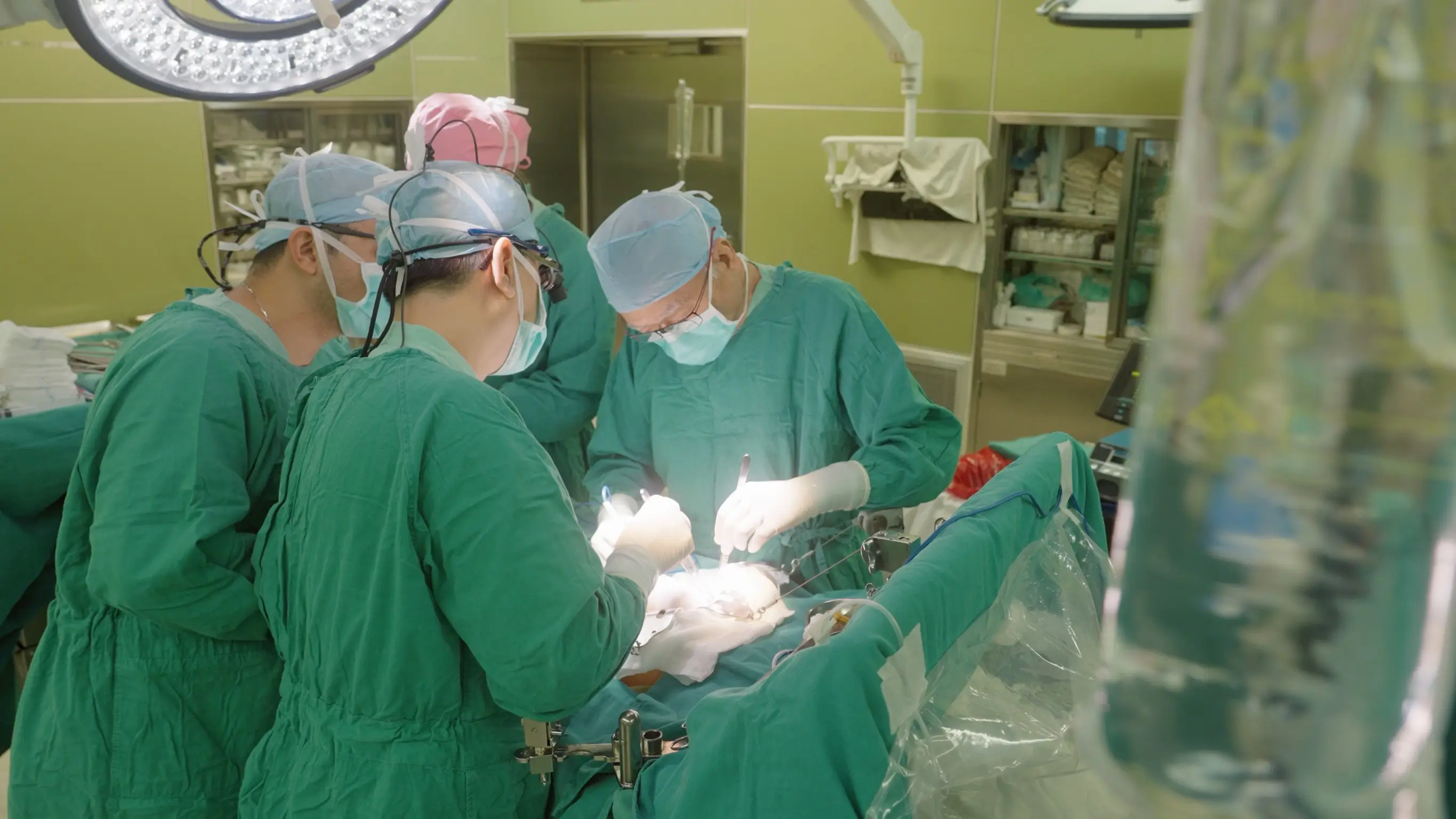
台灣拜耳2款造影劑不純物超標 食藥署:需回收逾1.8萬瓶


【記者賴昀岫/台北報導】知名藥廠出包!衛福部食藥署公告,台灣拜耳股份有限公司的2款造影劑「烏賴加芬76%」及「胃加芬液」,因不純物含量超出或趨近廠商自訂的規格上限情形,預防性回收20批,共計1萬8088瓶,目前均有其他藥品可替代。
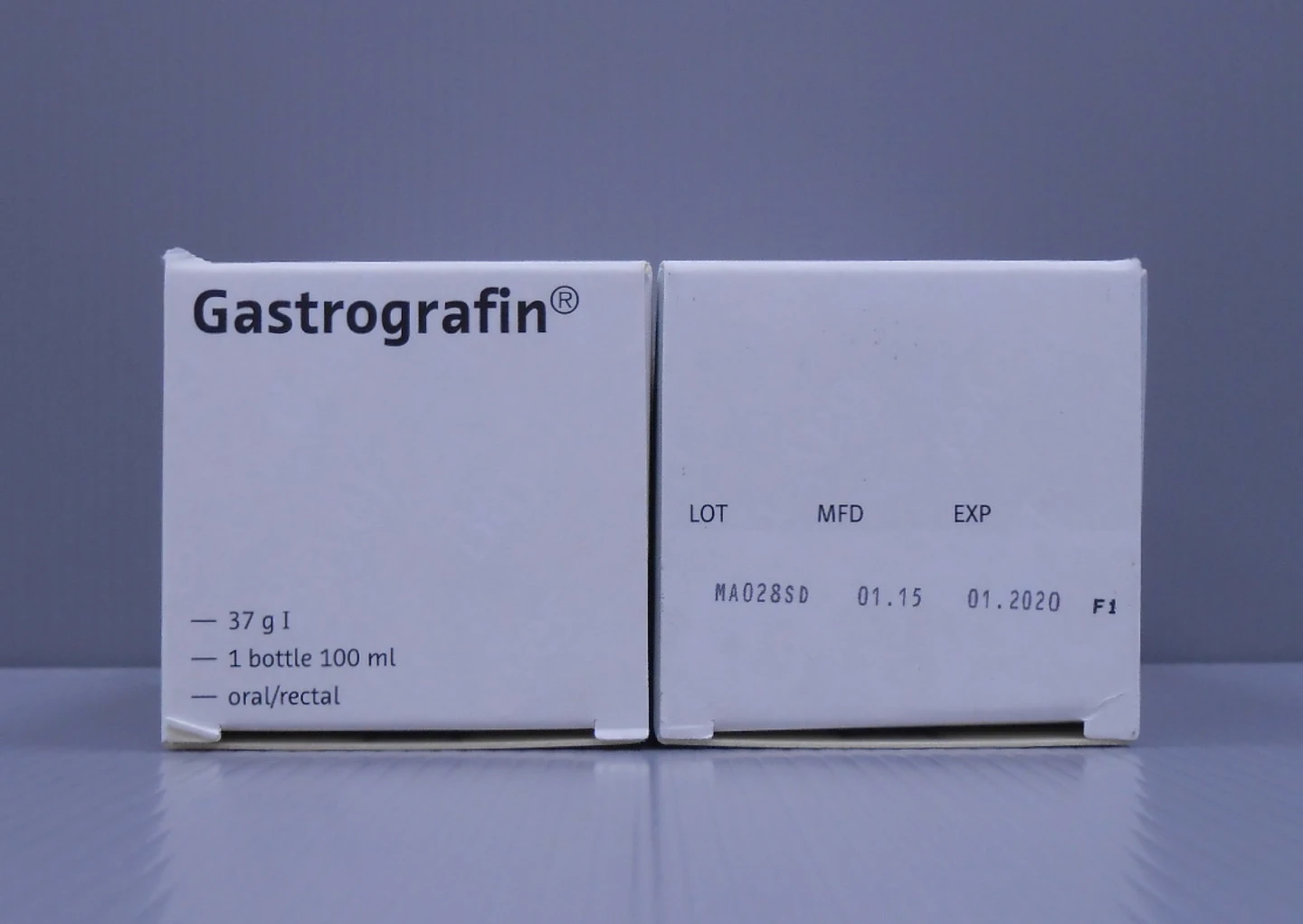
食藥署藥品組簡任技正劉佳萍說,食藥署在今年2月26日接獲台灣拜耳股份有限公司主動通報,「烏賴加芬76%(衛署藥輸字第000502號)」及「胃加芬液(衛署藥輸字第009313號)」,藥品中亞硝胺類不純物(N-Nitroso-Meglumine)含量,超出或趨近廠商自訂的規格上限,於3月16日發布藥品回收警訊。
2項藥品主成分皆為amidotrizoic acid,劉佳萍指出,「烏賴加芬76%」適應症為尿道、血管X光造影劑,國內尚有5張不同成分相似適應症的藥品許可證可替代;「胃加芬液」適應症為胃腸道放射檢驗用造影劑,國內尚有3張不同成分相似適應症之藥品許可證可替代,無藥品短缺之虞。


食藥署指出,藥品「烏賴加芬76%」,本次回收共12批,已銷售數量共計1萬2649瓶,回收批號為MAV43M6、MA043P2、MA04L2L、MA04NEJ、MA04SPR、MA04VPJ、MA03UBE、MA046FC、MA04H8S、MA04LH8、MA04LH9、MA04RLS。
藥品「胃加芬液」本次回收共8批,已銷售數量共計5439瓶,回收批號為MA04HF2 F1、MA04HF2 F2、MA04HF2 F3、MA04MPR F1、MA04MPR F2、MA04P3R F1、MA04S8L F1、MA04S8L F2。

劉佳萍說,食藥署已要求廠商於2026年4月4日前,完成回收作業並繳交調查報告,含不純物產生原因及預防矯正措施,如藥商未依規定辦理回收作業,將依《藥事法》91條,處新台幣20萬至500萬元罰鍰。
劉佳萍表示,不純物情形多在屆效期的安定性試驗中發現,其中「烏賴加芬76%」有效期間為5年、「胃加芬液」有效期間為4年,且案內不良品情形之批號藥品皆未輸台,但為了確保藥品品質及病人用藥安全,廠商主動辦理相關批號預防性回收。